

CLINICAL
RESULTS
Barrigel Pivotal試験の結果
治療プロトコル
治療プロトコル
寡分割放射線療法(HFRT)-効果的でより利便性が高い治療法
前立腺がんに対するHFRTの使用は、以下の理由で近年劇的に増加しています1
- 優れた腫瘍抑制効果
- 副作用の少なさ
- 通常分割放射線療法 (CFRT)と比較した際の
患者さんの利便性の高さ

HFRTでは、より少ない分割回数でより高い線量を照射することができますが、直腸が被爆のリスクにさらされていることに変わりはありません。HFRTでは通常分割放射線療法(CFRT)よりも急性グレード2以上の消化管毒性が強いことを考慮すると、直腸スペーシングは、この効果的で利便性の高い治療を受ける多くの患者にとって、臨床的に重要なニーズに応えられる可能性があります2。
Barrigel Pivotal試験は、寡分割放射線療法における直腸スペーシングに関する、FDAが審査した最初の無作為化対照試験です。
より良い結果を得るには
コントロールが重要です²
より良い結果を得るには
コントロールが重要です²
Barrigel は直腸への放射線量を臨床的に有意に低減させる効果があることが証明されています
Barrigel Pivotal試験では、98.5% の患者が
主要評価項目である
直腸V54 Gy*の少なくとも25%の減少を達成しました (p<0.001)
*54 Gyは60 Gyの90%に相当
- 放射線性直腸炎
- 下痢
- 痔
リスクを最小限に抑えるには
コントロールが重要です
リスクを最小限に抑えるには
コントロールが重要です
Barrigel Pivotal試験では、
- Barrigelと関連した有害事象はゼロ
- 周術期の有害事象はゼロ
- 直腸膨満感の有害事象はゼロ
- 処置後に直腸の痛みや不快感を訴える患者はゼロでした2
現在までに
- Barrigelに関連する有害事象の報告はゼロ3,4
- MAUDEデータベースにおける塞栓症の報告はゼロです4
初回から一貫して
対称的な留置が可能です
初回から一貫して
対称的な留置が可能です
Barrigelの初回留置-連続症例(同日内)
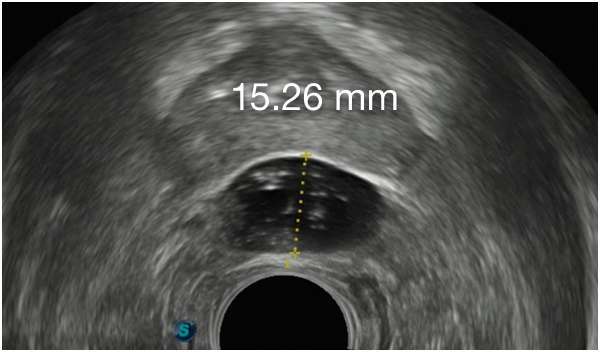
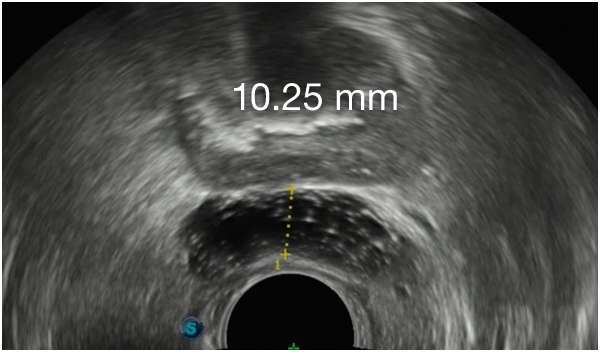
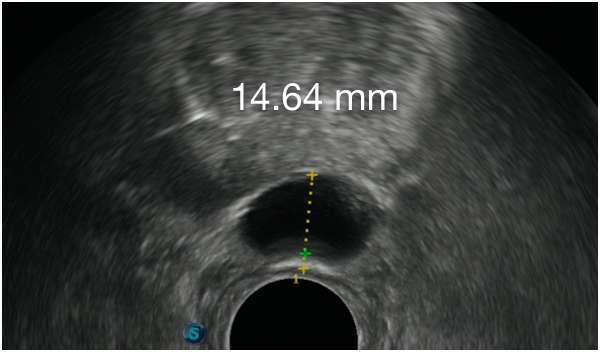
TRUS画像提供:Daniel R. Welchons, MD
Urologist; New York, United States
DR. WELCHONSの留置テクニック
直腸スペーシングでは
安定性が重要です
直腸スペーシングでは
安定性が重要です
吸収時にも安定したスペースが認められた
患者の例
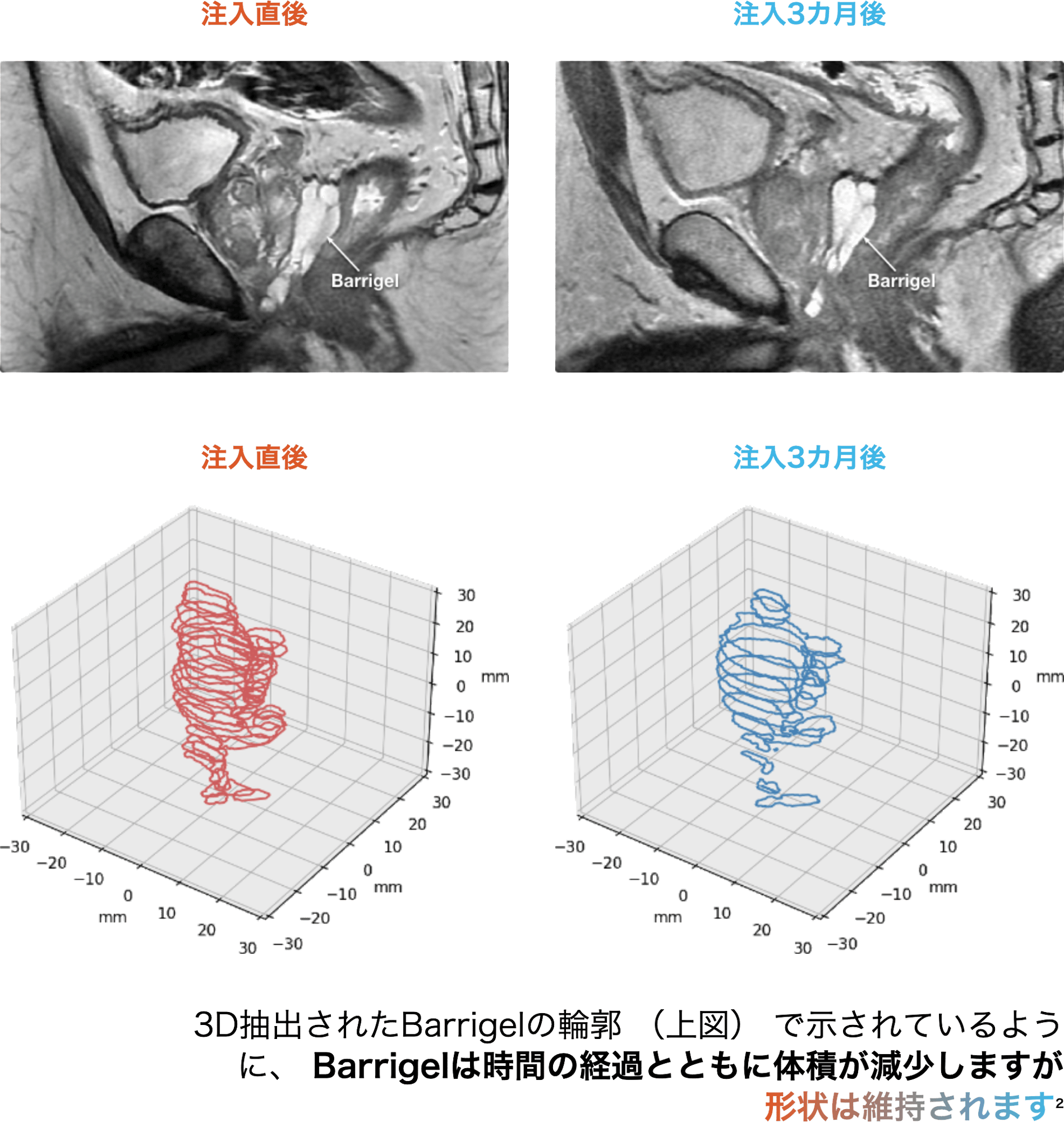


1. Dearnaley D, Syndikus I, Mossop H et al. Conventional versus hypofractionated high-dose intensity-modulated radiotherapy for prostate cancer: 5-year outcomes of the randomised, non-inferiority, phase 3 CHHiP trial. Lancet Oncol. 2016;17:1047–60.
2. Mariados NF, Orio PF III, Schiffman Z et al. Hyaluronic acid spacer for hypofractionated prostate radiation therapy: A randomized clinical trial. JAMA Oncol. 2023: e1-e8.
3. Data on file. Palette Life Sciences.
4. MAUDE Database. https://accessdata.fda.gov. Accessed 6/22/2023.